
Illustration: Marcelle Louw for GIJN
Ressource Guide
Enquêter sur la santé et la médecine
Ressource Guide Chapitre
Enquêter sur la santé: Préface
Ressource Guide Chapitre
Guide pour enquêter sur la santé: introduction
Ressource Guide Chapitre
Enquêter sur la santé et la médecine: Chapitre 1 – Développement et homologation des médicaments
Ressource Guide Chapitre
Enquêter sur la santé et la médecine: Chapitre 2 – Toutes les études ne se valent pas
Ressource Guide Chapitre
Enquêter sur la santé et la médecine: Chapitre 3 – Les bases scientifiques de l’influence
Ressource Guide Chapitre
Enquêter sur la santé et la médecine: Chapitre 4 – Couvrir la sécurité des médicaments
Ressource Guide Chapitre
Enquêter sur la santé et la médecine: Chapitre 5 – Pièges, battage médiatique et principes éthiques
Ressource Guide Chapitre
Enquêter sur la santé et la médecine: Glossaire, agences, et livres
Couvrir la sécurité des médicaments
Un produit pharmaceutique comme un médicament, un vaccin ou un dispositif médical, doit traverser les différentes phases de test puis passer par un processus d’homologation avec les organismes de réglementation pour pouvoir arriver sur le marché et être prescrit et vendu. Des effets indésirables graves peuvent apparaître lorsque le produit est largement utilisé pour la première fois par de vrais patients. Cela n’est pas uniquement dû aux failles potentielles de la recherche scientifique et aux problèmes liés à l’homologation et aux publications dans les revues scientifiques. C’est aussi parfois une question d’échelle : si vous testez l’innocuité sur 5000 patients, un événement indésirable survenant chez un patient sur 20.000 ne pourra devenir apparent que lorsqu’un nombre beaucoup plus important de patients utiliseront le produit. C’est pourquoi les dix premières années suivant l’homologation d’un médicament sont considérées comme particulièrement importantes pour détecter les effets indésirables.
Conseil 1 : Évaluez les preuves
Les rédacteurs en chef adorent les sujets liés aux dommages causés par les médicaments, les vaccins et les dispositifs médicaux, car ils sont populaires auprès du public. Il existe une pléthore de sujets potentiellement intéressants, mais de nombreux pièges subsistent et il est nécessaire que les journalistes mènent une enquête minutieuse.
Il faut commencer par développer une compréhension systématique du développement et des tests de médicaments, sans oublier de procéder à une revue de la littérature et des données annexes. Comme nous l’avons vu dans le premier chapitre, plusieurs milliers de personnes auront testé un produit médical dans un environnement contrôlé avant sa mise sur le marché. C’est pourquoi, en dépit des exceptions, les « nouveaux médicaments » sont généralement considérés comme moins sûrs que ceux qui sont plus anciens ; c’est tout simplement parce qu’on ne les comprend pas encore aussi bien sur le plan médical.
La phase que les agences de réglementation définissent comme « surveillance post-commercialisation » est importante. Elle comprend la pharmacovigilance, un type de surveillance que l’OMS définit comme « la science et les activités relatives à la détection, évaluation, compréhension et prévention des effets indésirables ou de tout autre problème lié au médicament. »
Lorsque la pharmacovigilance est basée sur la déclaration volontaire, cela peut représenter un problème majeur. Il existe plusieurs façons pour les médecins, le personnel infirmier, les pharmaciens et les patients de signaler les effets secondaires suspectés, notamment en les signalant directement aux autorités de réglementation. Si ces signalements sont jugés crédibles, les organismes de réglementation nationaux peuvent les transmettre au Programme de l’OMS pour la pharmacovigilance internationale (Uppsala Monitoring Centre) à Uppsala, en Suède. Les signalements ne sont pas publics. En tant que journaliste, vous pouvez seulement y avoir accès si un patient ou un médecin les partage avec vous. Les régulateurs peuvent fournir des statistiques à partir des signalements, mais même si les identifiants personnels sont masqués, les rapports complets sont toujours considérés comme hautement confidentiels.
La sous-déclaration des effets indésirables des produits médicaux constitue peut-être la faiblesse la plus préoccupante de ce système. Seule une infime fraction d’entre eux sont signalés, selon une revue systématique de 2006.
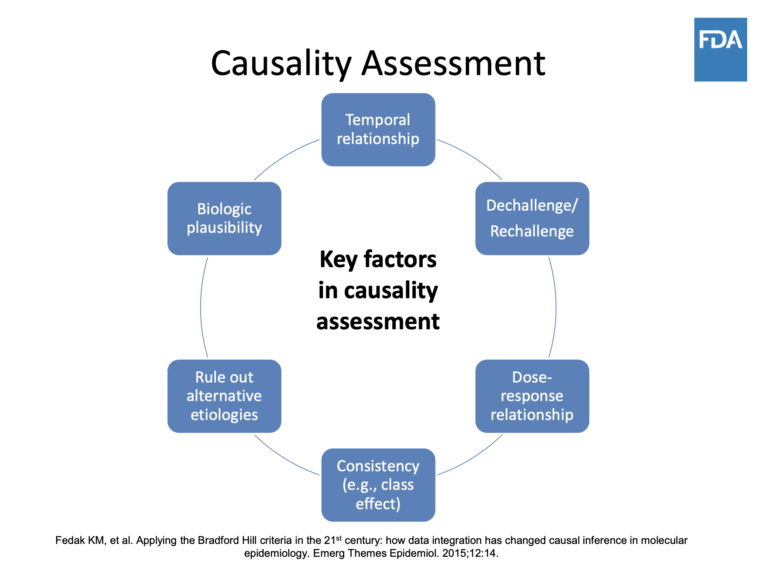
Prenez garde de ne pas vous fier à un seul signalement d’effet indésirable. Celui-ci est seulement un « signal » qui indique aux experts qu’ils doivent poursuivre leurs recherches sur un éventuel lien de causalité. De nombreux autres facteurs peuvent avoir contribué à l’effet signalé. Un seul signalement doit être évalué en conjonction avec d’autres preuves.
En règle générale, la couverture médiatique a un impact sur la déclaration des effets indésirables (appelés AER : Adverse Event Reporting). Si les médias rapportent les dangers présumés d’un médicament, dans les semaines qui suivent, les organismes de réglementation enregistreront une augmentation significative des signalements. Les effets signalés par les patients sont jugés de qualité inférieure à ceux consignés par les professionnels de la santé. Mais ils ont un réel potentiel pour améliorer le système, comme le souligne cet article : Patient reporting is the future of pharmacovigilance (Les déclarations des patients représentent l’avenir de la pharmacovigilance) que Sten Olsson a écrit alors qu’il était président de l’International Society of Pharmacovigilance. Gardez à l’esprit que le fait d’exposer des preuves n’entraînera pas nécessairement le retrait d’un médicament du marché. Les procédures réglementaires sont souvent plus compliquées. Votre enquête peut pousser les régulateurs à modifier la notice du médicament. Pendant ce processus, des négociations approfondies avec la société de commercialisation auront lieu.
Conseil 2 : Recueillez les données et interrogez les victimes
Il existe une grande différence entre les données de sécurité collectées lors du développement et de l’homologation et les données qui émergent après la commercialisation.
Tous les signalements sur les effets secondaires d’un médicament émanant d’un pays membre de l’OMS depuis 1968 sont stockés dans la banque de données VigiBase et restent disponibles, même si les produits ne sont plus sur le marché. Vous pouvez demander l’accès aux données disponibles en déposant une demande auprès des agences nationales de régulation.
Les données sont accompagnées de nombreuses mises en garde et sont difficiles à analyser, car un seul cas peut être enregistré sous plusieurs codes différents. En outre, les enquêtes sur la santé ont besoin d’êtres humains en chair et en os qui témoignent des dommages ou des préjudices qu’ils ont subis. Les « rapports de cas » sont toujours anonymes, de sorte que lorsque vous recevez des données des agents de pharmacovigilance, vous devez élaborer une stratégie pour identifier ces victimes présumées. Une astuce est de passer par l’intermédiaire des médecins : ils peuvent avoir un patient qui est prêt à parler aux journalistes. Ou ils peuvent connaître un autre médecin dont le patient a ressenti cet effet secondaire.
Vous pouvez avoir recours au « crowdsourcing » (enquête participative) en lançant un appel à témoin sur les réseaux sociaux, sur votre site web ou via la newsletter du média pour lequel vous travaillez. Pensez à indiquer clairement que vous étudiez le préjudice potentiel, ou l’expérience des patients concernant un produit pharmaceutique. L’appel à témoin exposera votre projet en cours mais vous aidera à entrer en contact avec des protagonistes potentiels.
newsletter du média pour lequel vous travaillez. Pensez à indiquer clairement que vous étudiez le préjudice potentiel, ou l’expérience des patients concernant un produit pharmaceutique. L’appel à témoin exposera votre projet en cours mais vous aidera à entrer en contact avec des protagonistes potentiels.
Imaginons donc que vous soyez tombé sur un produit potentiellement dangereux et que vous ayez même identifié des témoins potentiels pour votre article, des patients qui auraient subi les effets indésirables de ce produit. Que faites-vous après ? La clé est d’évaluer les preuves de manière indépendante et de comparer vos résultats avec les études publiées dans les revues.
Souvent, les expériences des victimes n’ont pas été signalées du tout. Raconter leurs histoires peut susciter d’autres témoignages de la part de patients ou de familles qui contacteront votre rédaction.
Rassemblez tous les cas, avec les détails médicaux, et n’oubliez pas de demander de signer une autorisation de levée du secret médical. Sans elle, votre enquête sera retardée. Les médecins et les hôpitaux refuseront de répondre à vos demandes tant que vous ne l’aurez pas obtenue. Ayez en tête que les lois nationales protègent la confidentialité des informations médicales des patients et que certaines sont assez strictes.
Lorsque vous avez dressé un tableau complet composé de cas spécifiques, présentez les preuves aux régulateurs. L’expérience a montré à maintes reprises qu’il est utile de les contacter avant la fin de votre enquête et bien avant la publication. Si vos méthodes sont solides et que vous avez découvert des faits qui sont d’intérêt public, il est dans l’intérêt des régulateurs de soutenir votre travail dans la mesure du possible. Bien sûr, ils ne vous donneront pas les noms des patients ou des informations qui les présentent sous un mauvais jour. Mais ils peuvent vous rendre attentif à certains aspects que vous pourriez avoir sous-estimés (par exemple, une étude, des données ou une règle spécifique s’appliquant à votre cas). Cela vous aidera à éviter les erreurs dans vos sujets. Parfois, ils peuvent même faire allusion à la société pharmaceutique ou à la société savante ayant joué un rôle en retardant ou en gênant le travail des régulateurs. L’industrie pharmaceutique utilise quand à elle souvent une stratégie de surcharge d’informations lorsqu’elle répond aux requêtes des journalistes d’investigation. Attendez-vous à de longues déclarations et des références à des études remplies de jargon scientifique.
Notre enquête Mourir pour quelques boutons pour la chaîne publique suisse RTS sur les effets secondaires psychiatriques du médicament contre l’acné Accutane, a déclenché une vague d’envois de témoignages de patients et de leurs proches. Sur les plus de 300 signalements que nous avons reçus, 61 cas ont été inclus par l’agence de réglementation suisse Swissmedic dans la base de données nationale et mondiale sur la sécurité des médicaments. L’agence a également publié une mise à jour à l’intention des prescripteurs et des patients sur les risques psychiatriques du médicament.
De même, l’enquête sur les dispositifs médicaux menée par Jet Schouten, journaliste de l’association d’audiovisuel public néerlandaise AVROTROS qui a inspiré le projet ICIJ Implant Files a été lancée après les nombreux témoignages reçus suite à la publication de son premier article.
Identifier des sources dans le cadre d’une enquête peut s’avérer compliqué. Le crowdsourcing et les recherches sur les réseaux sociaux sont incontournables. Vous pouvez utiliser des outils de recherche avancés comme ceux répertoriés dans le guide pour enquêter en ligne de GIJN.
Les procédures judiciaires peuvent également constituer une mine d’informations : elles peuvent vous permettre de repérer des sources, en particulier si vous enquêtez sur des effets graves et des dommages.
Se rapprocher de ses sources n’est jamais une bonne idée. Lorsque vous enquêtez sur la sécurité des médicaments, il faut absolument l’éviter. Lorsque vous êtes face à des cas d’injustice, des patients qui n’étaient pas correctement informés, des régulateurs qui étaient au courant mais n’ont rien fait, des conflits d’intérêts potentiels ou réels et des experts hautement compétents et très réputés, il est tentant de se reposer de manière excessive sur une ou deux sources. Mais votre devoir est d’évaluer les preuves et de dénoncer les actes répréhensibles, pas de vous faire de nouveaux amis.
Il est également important d’utiliser un langage prudent et précis et de ne pas monter en épingle votre sujet sur la sécurité d’un médicament. Un vocabulaire alarmiste qui simplifie le rapport bénéfice/risque et déforme les preuves scientifiques donnera aux autorités l’opportunité d’ignorer la question. Des sujets de mauvaise qualité peuvent même empêcher l’intervention des autorités réglementaires. Il se peut que des patients cessent de prendre un médicament sans en parler à leur médecin, ce qui pourrait être dangereux pour leur santé. L’emballement médiatique peut entraîner des actes qui ne sont pas fondés sur des preuves, comme retirer un médicament du marché au lieu de modifier les directives de prescription pour s’assurer qu’il sera pris correctement.
Conseil 3 : Exposez la fraude, l’inconduite scientifique et les mauvaises pratiques médicales
Des maisons de retraite aux laboratoires de recherche, des hôpitaux publics aux cabinets médicaux, le domaine de la santé est affecté par la fraude et les mauvaises pratiques médicales. De nombreux cas n’auraient jamais été rendus publics si certains actes répréhensibles n’avaient pas été exposés par des victimes, des procureurs, des défenseurs des droits humains et des journalistes. Certains de ces travaux sont inspirants et instructifs.
Dans certains cas, il était nécessaire de travailler de manière anonyme. En 1887, la journaliste américaine Nellie Bly s’est ainsi fait passer pour une malade mentale pour pouvoir enquêter sur des allégations de brutalité et de négligence dans une institution psychiatrique de New York. Cent ans plus tard, Naziha Syed Ali s’est rendue incognito au Pakistan, elle aussi, dans le but d’enquêter sur le trafic d’organes pour son enquête Doctors, Police and Middlemen (Médecins, police et intermédiaires). Une équipe de la BBC Africa Eye dirigée par Solomon Serwanjja a fait de même avec Stealing from the Sick (Dépouiller les malades), une enquête révélant le marché noir des produits pharmaceutiques en Ouganda.
Les témoignages des victimes jouent un rôle essentiel, comme dans l’enquête que Deborah Cohen de la BBC a réalisé sur les expériences sur les cellules souches, ou encore dans l’enquête de la Fondation Thomson Reuters menée par Roli Srivastava Missing Wombs: The Health Scandal Enslaving Families in Rural India (Les utérus manquants : le scandale sanitaire qui asservit les familles en milieux ruraux en Inde).
Les erreurs médicales peuvent être analysées en combinant les données avec les témoignages des victimes : c’est l’objectif poursuivi par le média péruvien Ojo Público avec le projet Cuidados Intensivos. Vous pouvez aussi lire l’enquête de Leonid Schneider, journaliste et ancien biologiste moléculaire, sur un cas présumé d’inconduite scientifique impliquant des greffes de trachée. L’affaire a aussi été couverte dans le documentaire de Benita Alexander intitulée « He Lied About Everything » (Il a menti sur tout) produit par Discovery ou encore dans le documentaire en trois parties de Bosse Lindquist intitulé « The Experiments »(Les expériences) (SVT). Vous pouvez aussi lire Tide of Lies (Marée de mensonges) de Kai Kupferschmidt à propos du long périple de la chercheuse Alison Avenell qui a exposé les dessous d’une importante affaire de fraude scientifique. Cet ouvrage met en évidence les nombreux problèmes qui affectent les revues biomédicales.
L’enquête détaillé de Sushma Subramanian publiée dans Slate, Worse Than Tuskegee (Pire que Tuskegee) est l’occasion de découvrir un exemple inquiétant : la façon dont, dans les années 1940, des chercheurs américains ont infecté des Guatémaltèques avec la syphilis et la gonorrhée, avant de les abandonner sans traitement. L’affaire a été révélée en 2003 grâce à Susan Reverby, historienne au Wellesley College. John Carreyrou journaliste du Wall Street Journal, lauréat d’un prix Pulitzer en 2015 pour sa série Medicare Unmasked (Medicare démasqué), a entrepris la même année une enquête d’impact sur la société de tests sanguins Theranos. Celle-ci a abouti à une nouvelle série, sur fond d’accusations, et la publication de son livre « Bad Blood: Secrets and Lies in a Silicon Valley Startup » (Mauvais sang : secrets et mensonges dans une start-up de la Sillicon Valley).
De nombreuses enquêtes attendent toujours d’être menées dans le domaine dit de la « criminalité des entreprises ». Voici à ce propos, deux références qui vous assureront des nuits blanches. L’ouvrage de Peter C. Gøtzsche intitulé « Médicaments mortels et crimes organisés » dont vous pouvez lire un extrait dans le BMJ : Big Pharma often Commits Corporate Crime, and this must be Stopped (Les lobbies pharmaceutiques commettent des crimes et cela doit cesser. Vous pouvez également lire Twenty-Seven Years of Pharmaceutical Industry Criminal and Civil Penalities: 1991 through 2017 (Vingt-sept ans de sanctions pénales et civiles pour l’industrie pharmaceutique : de 1991 à 2017) de Public Citizen.