Recursos Guía
Guía para periodistas que investigan salud y medicina
Recursos Guía Capítulo
Guía de GIJN sobre investigación periodística en salud y medicina – Prefacio
Recursos Guía Capítulo
Guía de GIJN sobre investigación periodística en salud y medicina: Capítulo 1
Recursos Guía Capítulo
Guía de GIJN sobre investigación periodística en salud y medicina: Capítulo 2
Recursos Guía Capítulo
Guía de GIJN sobre investigación periodística en salud y medicina: Capítulo 3
Recursos Guía Capítulo
Guía de GIJN sobre investigación periodística en salud y medicina: Capítulo 4
Recursos Guía Capítulo
Guía de GIJN sobre investigación periodística en salud y medicina: Capítulo 5
Recursos Guía Capítulo
Guía de GIJN sobre investigación periodística en salud y medicina: Apéndice
Regulación de medicamentos: desarrollo y autorización
Primera sugerencia: profundiza en el desarrollo y la aprobación
Si tu historia trata el tema de los medicamentos, es esencial profundizar en su desarrollo y aprobación. Aunque todos los países tienen su propia agencia reguladora (véase en el apéndice), el trabajo de la Agencia Estadounidense de Alimentos y Medicamentos (FDA, Food and Drug Administration) y la Agencia Europea de Medicamentos (EMA, European Medicines Agency) tienen una gran influencia en el mercado farmacéutico mundial.
Las pruebas presentadas por la industria farmacéutica a las agencias reguladoras para demostrar la seguridad y eficacia del producto suelen ser públicas y estar disponibles en sus sitios web.
El proceso de desarrollo y aprobación de medicamentos se desarrolla en cinco fases, que se muestran en la siguiente ilustración:

Ilustración: Re-Check.ch
Es esencial profundizar en todas estas fases, comenzando por los ensayos clínicos aleatorizados (ECA) –conocidos con el nombre «patrón oro»–, que se realizan durante las fases II y III. Ahí es donde se encuentra la mejor evidencia disponible —con frecuencia mejor que la que se difunde cuando el producto entra en el mercado–. Sin embargo, los ECA incluso pueden llegar a ser “trucados” para engañar.
Por lo tanto, el periodismo médico de investigación no debe centrarse solo en la corrupción financiera o en los efectos adversos de los medicamentos o de los dispositivos, también debe preguntarse si los ensayos clínicos están sesgados, si no se han publicado por dar resultados negativos o si son mal interpretados.
De hecho, algunos de los ECA más citados y publicados en prestigiosas revistas médicas han sido inexactos. Para más información, lee el influyente artículo de John P. A. Ioannidis: “Por qué la mayor parte de los hallazgos de investigación publicados son falsos” (Why Most Published Research Findings Are False). En resumen, en las fases iniciales son más rigurosos y reveladores los métodos y resultados.
La etapa de autorización crea una gran tensión entre los intereses públicos y privados (comerciales). El fabricante tratará de ejercer la máxima influencia sobre los reguladores, cuya decisión determinará, no solo si el medicamento puede ser comercializado, sino también los usos/indicaciones para los que puede ser vendido. Aparte, las empresas farmacéuticas suelen inundar a los reguladores con una gran cantidad de documentos. Aunque esto puede parecer conveniente, en algunos casos hace que el trabajo de las agencias sea más difícil, ya que sus capacidades son limitadas.
El primer paso es echar un vistazo a todos los detalles del proceso de autorización y evaluar si se han cumplido las normas o si el patrocinador obtuvo condiciones especiales, a manera de excepción o de concesiones particulares. Por ejemplo, los reguladores pueden haberle permitido a la compañía demostrar la eficacia del fármaco con base en resultados intermedios y no en su eficacia en el resultado principal/final.
Los resultados intermedios (o criterios de valoración sustitutos) son indicadores (a menudo biomarcadores, como los análisis de sangre) elegidos por los investigadores, porque se consideran importantes en el mecanismo de una enfermedad. Por ejemplo, la presión arterial puede usarse como resultado intermedio sustitutivo en un ensayo sobre medicamentos cardiovasculares, ya que es un factor de riesgo conocido para ataques cardíacos y accidentes cerebrovasculares.
La hipótesis es que si el fármaco muestra un efecto en el resultado intermedio (como la presión arterial alta), también lo tendrá en el resultado clínico (como ataques cardíacos y accidentes cerebrovasculares). Desafortunadamente, el efecto de un fármaco sobre un resultado intermedio muchas veces no traerá el beneficio esperado por los pacientes; incluso, puede dañarlos. De paso, los resultados intermedios solo evalúan el beneficio sin abordar el daño.
Por lo tanto, un medicamento para la diabetes podría ser dañino pero eficaz para reducir la glucemia, el azúcar en sangre. Un resultado intermedio para los diabéticos, que tienden a morir de ataques cardíacos y accidentes cerebrovasculares. Ese mismo fármaco podría matar a más pacientes al dañar su hígado, porque otros aspectos no fueron descubiertos o entendidos. Por esta razón, deben valorarse con precaución las conclusiones de los estudios diseñados sobre resultados intermedios.
El sitio web Students 4 Best Evidence (S4BE) es un buen recurso para aprender lo básico en este campo, porque es preciso y comprensible para los no científicos. S4BE explica las dificultades de los “resultados intermedios (sustitutos)” con un ejemplo clásico de la década de 1970: “Los pacientes que sufren de arritmia (latidos cardíacos irregulares) suelen recibir fármacos antiarrítmicos para ‘corregir’ el latido del corazón y que vuelva el ritmo a la normalidad. La arritmia es una condición peligrosa, ya que aumenta el riesgo de muerte súbita cardíaca. En la década de 1970, un equipo de investigadores estaba estudiando un nuevo grupo de medicamentos antiarrítmicos y los resultados iniciales sugirieron que estos fármacos lograban la normalización del latido cardíaco. Sin embargo, los resultados finales demostraron que hubo una mayor tasa de mortalidad en el grupo que recibió los fármacos antiarrítmicos en comparación con el que tomó el placebo. Por tanto, fue engañoso medir el resultado según el control del ritmo de los latidos cardíacos y los fármacos habían estado haciendo más daño que beneficio.

Una vez que se han recogido y analizado los resultados de los ensayos clínicos, es crucial comparar los datos publicados por las agencias con la literatura científica médica. Verifica la consistencia y las discrepancias, y presta atención a cada estudio presentado a los reguladores. Se puede descubrir que un estudio que desempeñó un papel relevante en el proceso de aprobación nunca fue divulgado en una revista científica y esto suele ser una señal de alerta porque no todos los resultados que las agencias obtienen han sido o serán publicados. Los fabricantes aseguran que los resultados favorables se difunden en revistas científicas, pero no siempre ocurre en el caso de resultados desfavorables.
Hay un caso famoso en que los datos no publicados presentados a un regulador fueron pasados por alto con consecuencias perjudiciales. El analgésico Vioxx (rofecoxib) había sido un éxito rotundo para Merck hasta que en 2004 llegaron los resultados impactantes de David Graham, un científico de la FDA. El fármaco Vioxx aumentaba considerablemente el riesgo de ataques cardíacos. Graham estimó que hubo hasta 140.000 ataques cardíacos y 60.000 muertes debido a sus efectos secundarios. La compañía retiró voluntariamente el medicamento del mercado, mientras se difundían las revelaciones de Graham. El Wall Street Journal informó que al menos desde 2000 –cuatro años antes de sacar el medicamento al mercado– Merck sabía que Vioxx aumentaba el riesgo de ataques cardíacos y muertes, pero optó por no revelar los datos. Además, los documentos filtrados de la compañía demostraron cómo Merck instruyó a sus representantes de ventas para evitar iniciar discusiones sobre estos efectos secundarios con los médicos prescriptores.
Un estudio de diciembre de 2004, publicado en The Lancet por el epidemiólogo suizo Peter Jüni y sus colegas de la Universidad de Berna, demostró que la FDA debería haber conocido los peligros de Vioxx, porque parte de los datos preocupantes e inéditos se habían presentado al regulador estadounidense. Jüni y sus colegas escribieron: “nuestros hallazgos indican que el rofecoxib debería haber sido retirado varios años antes. Hay que aclarar las razones por las que el fabricante y las autoridades para el control de medicamentos no valoraron y sintetizaron continuamente las pruebas acumuladas”.
El caso Vioxx provocó titulares en todo el mundo y causó una avalancha de demandas, cerradas por Merck con acuerdos récord. El caso también se convirtió en un ejemplo de hasta qué punto pueden ir mal las cosas. Entre los muchos recursos disponibles sobre la saga de Vioxx vale la pena destacar la serie especial de NPR: Vioxx: La caída de un medicamento; la transcripción del testimonio de David Graham ante el Senado de los Estados Unidos y el artículo de BMJ ¿Qué hemos aprendido de Vioxx?
Otro ejemplo de publicación selectiva de pruebas relevantes de la industria farmacéutica es el caso del analgésico OxyContin, comercializado por Purdue Pharma, que se ha convertido en emblema de la crisis estadounidense de los opioides. Purdue Pharma sabía del abuso excesivo de su medicamento en los primeros años, tras la aprobación de su comercialización en 1995, y la compañía ocultó la información, como han demostrado las investigaciones del periodista Barry Meier.
Meier comenzó a cubrir la comercialización del analgésico OxyContin y la epidemia resultante de adicción a los opioides desde 2001 para el periódico New York Times. Investigó durante años y escribió un libro sobre el tema que fue publicado por primera vez en 2003, con una versión actualizada en 2018: Analgésicos: Un imperio del engaño y el origen de la epidemia de opioides de América. En octubre de 2020, el Departamento de Justicia de Estados Unidos anunció la conclusión de sus investigaciones penales y civiles contra Purdue Pharma, con sentencia de culpa y un acuerdo federal de 8.000 mil millones de dólares.
Aunque estos casos –y otros similares– demuestran los límites del trabajo de las agencias reguladoras, los estándares del regulador federal estadounidense (FDA) están entre los más estrictos y exigentes del mundo. La agencia produce mucha documentación, gran parte de ella publicada en su sitio web. Es una fuente útil si quieres entender cómo un producto llega al mercado. En cualquier página sobre un fármaco concreto se encuentra la cronología con enlaces a las piezas relevantes de los estudios utilizados durante el largo proceso de lanzar un medicamento a la venta.
Hay que prestar especial atención a las cartas de aprobación de la FDA y a las revisiones clínicas y estadísticas. Pero conviene tener en cuenta que el trabajo de la FDA no es perfecto y que la agencia depende de la industria farmacéutica para una gran parte de su financiación.
Como se señaló en una investigación de 2016 del Proyecto de Supervisión del Gobierno (POGO), la FDA depende cada vez más de la financiación de la industria y el dinero está vinculado a ciertas condiciones. Durante las dos décadas estudiadas el presupuesto de la FDA para “revisión de aplicaciones de medicamentos humanos” bajo la “Ley de tasas de medicamentos de prescripción (Drug Prescription User Fee Act)”, los pagos de las industrias, como tales tasas, pasaron a financiar el presupuesto de la FDA del 35% al 71%. Esta dependencia y el claro conflicto de intereses aumenta la influencia del “Big Pharma”, concluyó POGO. Hay indicios de que el trabajo de la FDA puede estar cada vez más comprometido. Así lo demuestra la tendencia a bajar las exigencias para la aprobación de medicamentos, por ejemplo, al ampliar los criterios para que un producto sea aprobado a través del proceso “exprés”.
La “vía rápida” fue creada con un doble propósito: introducir nuevos tratamientos para las necesidades no cubiertas de los pacientes. Para ello, se implantó un procedimiento especial que acelera la aprobación al reducir la cantidad y la calidad de las pruebas que la industria debe presentar. Sin embargo, la “vía rápida” se convirtió en los últimos años en un atajo para las empresas farmacéuticas, que les permite saltar o acortar evaluaciones en profundidad por parte de los reguladores.
Otras cuestiones que requieren nuestra atención al investigar fármacos son descritas por Donald W. Light, Joel Lexchin y Jonathan J. Darrow en Institutional Corruption of Pharmaceuticals and the Myth of Safe and Effective Drugs, un artículo de 2013 publicado en Journal of Law, Medicine & Ethics. En su lista de problemas incluye el hecho de que la mayoría de los medicamentos nuevos aprobados por la FDA desde la década de 1970 no son mejores para los pacientes que los medicamentos más antiguos y que el nivel de «seguridad» es bajo, dado que han causado una epidemia indiscutible de efectos secundarios dañinos, incluso cuando se prescriben de forma adecuada.
La investigación en los archivos de la FDA y la EMA (European Medicines Agency) puede aportar grandes beneficios para tu trabajo. Si bien la FDA publica bastantes documentos, la EMA puede ser un recurso muy interesante, por ejemplo, para acceder al informe del ensayo clínico de un fármaco. Como afirman los investigadores Peter Doshi de la Universidad de Maryland y Tom Jefferson de la Universidad de Oxford: «trata los informes de ensayos clínicos y otras partes del expediente presentado por los patrocinadores como información comercial confidencial y, por lo tanto, no se puede divulgar en virtud de la Ley de Libertad de Información de los Estados Unidos». Por el contrario, la EMA interpreta que los documentos –incluidos los informes de ensayos clínicos– estarán sujetos a su política de libertad de información «reactiva» y es el único regulador en el mundo que da acceso a estos datos de forma rutinaria. Sin embargo, la agencia se ocupa de un número enorme y creciente de solicitudes de acceso.
Los ciudadanos de la Unión Europea y las personas (físicas o jurídicas) que residan o tengan su domicilio social en un Estado miembro de la UE tienen derecho a acceder a los documentos de la EMA. Los detalles sobre el procedimiento para obtener información están disponibles en su página web.
Doshi y Jefferson, que tienen una enorme experiencia con este proceso, subrayan que «puede tardar un tiempo considerable en lograrse el acceso y, a menudo, solo se logra después de una larga correspondencia». Además, las empresas farmacéuticas pueden oponerse a que la EMA divulgue datos de ensayos clínicos y, a veces, el conflicto puede terminar en los tribunales, como se demostró en un caso de 2018 que involucra la publicación por parte de la EMA de informes de estudios clínicos sobre un medicamento para la distrofia muscular de Duchenne.
Las agencias reguladoras son criticadas con regularidad por su cercanía a la industria. Esto también se aplica a la EMA, a pesar de que la agencia ha hecho algunos esfuerzos para aumentar su transparencia en la comunicación sobre conflictos de intereses.
Además de las agencias nacionales, las organizaciones internacionales también juegan un papel en la regulación de medicamentos y dispositivos médicos, incluyendo certificación, fabricación, distribución, precios, comercialización, investigación y desarrollo y derechos de propiedad intelectual. Vale la pena profundizar en tu trabajo si deseas comprender la regulación y aprobación de un medicamento. Puede ayudarte el hacer la pregunta correcta con respecto a cuestiones clave como:
- ¿Por qué las autoridades reguladoras exigieron unos datos y no otros?
- ¿Cómo afecta la propiedad intelectual del producto a sus licencias y mercados?
- ¿Intentó la industria farmacéutica influir en el trabajo de alguna de estas organizaciones?
Aquí hay algunas agencias que se pueden consultar. Cada una de ellas tiene una amplia gama de competencias que cubren diferentes aspectos de este mercado y que se describen en detalle en sus sitios web:
- Consejo Internacional para la Armonización de Requisitos Técnicos para Productos Farmacéuticos de Uso Humano (ICH)
- Organización Panamericana de la Salud (OPS)
- Organización Mundial del Comercio (OMC)
- Organización Mundial de la Propiedad Intelectual (OMPI)
- Organización Mundial de la Salud (OMS)
Investigación de dispositivos médicos
Los dispositivos médicos comprenden una amplia gama de equipos, definidos por Daniel B. Kramer y sus colegas como «tecnologías de salud que no son medicamentos, vacunas o procedimientos clínicos». Investigarlos significa lidiar con un entorno poco regulado. Es innegable que en las últimas décadas se han introducido nuevos dispositivos como mejores alternativas para algunas condiciones, pero no siempre ofrecen beneficios a los pacientes y, en ciertos casos, los han expuesto a riesgos sustanciales, como lo demuestra la retirada de varios implantes mamarios y prótesis de cadera.
Las normas en este ámbito son más tolerantes que las aplicables a los productos farmacéuticos.
En 2016, la revisión Drugs and Devices: Comparison of European and US Approval Processes demostró que solo alrededor de 2% de los dispositivos médicos aprobados en los últimos años pasaron por “Solicitud de Aprobación de Comercialización” (Premarket Approval Application), el proceso más riguroso de la FDA para la aprobación de dispositivos. La revisión, publicada en JACC: Basic to Translational Science, demostró que solo entre 10% y 15% de las presentaciones de dispositivos de la FDA contenía datos clínicos y que 7% estaba exento de revisión. «Cuando se requieren ensayos clínicos para los dispositivos, con frecuencia no cumplen los mismos estándares estrictos de evidencia clínica que se requieren para los medicamentos», encontró la revisión. «A menudo no son aleatorizados, no tienen grupos de control activos y carecen de criterios de valoración concretos».
Los procesos de aprobación de dispositivos médicos en la Unión Europea y los Estados Unidos comparten algunas similitudes. Pero también existen diferencias críticas, como lo demostró la misma revisión: “antes de la aprobación de un dispositivo médico en los Estados Unidos, debe demostrarse que es seguro y eficaz. Los dispositivos médicos aprobados en Europa solo tienen que demostrar seguridad y rendimiento. Un efecto colateral de las normativas europeas más laxas desde el punto de vista comercial es la aprobación inicial en Europa de dispositivos respaldados por empresas estadounidenses, antes de su presentación en los Estados Unidos».
Estados Unidos y Europa lideran el mercado y, aunque los reguladores nacionales tienen sus propios procesos de aprobación para dispositivos médicos, la mayoría de los países tiende a seguir la normativa de la FDA y la EMA. En muchos casos, el proceso suele ser más corto para un dispositivo médico concreto si ya ha sido aprobado por la FDA y la EMA.
Sin embargo, existe preocupación creciente sobre la idoneidad y la eficacia de ambos procesos de aprobación, como se demostró en la revisión de 2012 de Daniel B. Kramer, Shuai Xu y Aaron S. Kesselheim, ¿Cómo funciona la regulación de dispositivos médicos en los Estados Unidos y la Unión Europea? Una revisión sistemática. «Los estudios sobre la aprobación de dispositivos de los Estados Unidos y la Unión Europea, y los resultados de las evaluaciones posteriores a la comercialización, sugieren que son necesarias reformas profundas de ambos sistemas, incluida la mejora de la clasificación de dispositivos en los Estados Unidos y la promoción de la transparencia y la supervisión posterior a la comercialización en la UE».
En 2014, Carl Heneghan –científico de Oxford– se unió a una investigación “ficticia” para demostrar que la regulación era tan laxa que el envasado de fruta podría ser aprobado como un dispositivo médico. Jet Schouten, periodista de la cadena pública holandesa AVROTROS, pidió a Heneghan que presentara un informe científico ficticio sobre la reutilización de las mallas empleadas en la venta de mandarinas como malla quirúrgica transvaginal, que normalmente se usa para reforzar el tejido debilitado en la zona pélvica. Y tuvieron éxito: los reguladores no anticiparon problemas en el proceso de aprobación y no se hicieron preguntas sobre seguridad.
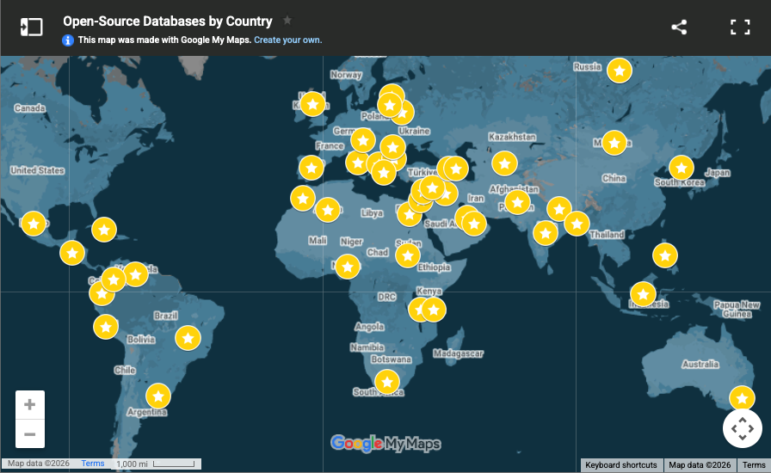
Cinco años después, se logró obtener más conocimiento sobre los dispositivos médicos debido a la investigación Implant Files del Consorcio Internacional de Periodistas de Investigación (ICIJ), inspirado en el trabajo de Schouten. El proyecto descubrió que las autoridades sanitarias no protegen a los pacientes de los dispositivos médicos que se han relacionado con más de 83.000 muertes y más de 1,7 millones de lesiones en la última década. El ICIJ publicó una base de datos internacional de dispositivos médicos accesible al público, que contiene informes de productos, alertas y avisos de seguridad sobre el terreno, datos extraídos de fuentes públicas y respuestas a solicitudes de acceso a la información.
La colaboración del ICIJ implicó a 36 países, más de 250 periodistas y especialistas en datos de 58 organizaciones de medios de comunicación. Desde que se publicó Implant Files los reguladores del mundo se han comprometido a mejorar la supervisión de los dispositivos médicos.
Para obtener más información sobre este proyecto de ICIJ y las herramientas que el equipo global utilizó y desarrolló, consulta en ICIJ Everything You Need to Know About the Implant Files y Lessons from Inside the Implant Files. La base de datos y las herramientas son buenos recursos para los periodistas que investigan historias relacionadas.
Segunda sugerencia: presta atención a los signos de alerta
Durante el proceso de aprobación de un fármaco, las empresas farmacéuticas utilizan múltiples técnicas para lograr una resolución favorable. Las estrategias de marketing y la creciente medicalización se utilizan para interferir con el proceso de aprobación. Veamos tres de las estrategias que utilizan:
- Ampliar la definición de los riesgos o enfermedades a tratar para ampliar el valor potencial del fármaco. Vea estos ejemplos clásicos de colesterol, presión arterial y glucosa en la sangre.
- Intervenir y detectar antes: los ejemplos típicos son exámenes preventivos de cáncer, chequeos de salud y pruebas genéticas. Sobre el tema recomendamos:
-
- Chequeo. Cómo el sobre- diagnóstico y otros daños pueden socavar los beneficios (Screening: How Overdiagnosis and Other Harms Can Undermine the Benefits) de Health News Review.
- Poner a prueba las pruebas. Muchos procedimientos médicos son innecesarios y con riesgos (Putting Tests to the Test: Many Medical Procedures Prove Unnecessary — and Risky) de Scientific American.
- Los 200 mil millones de dólares de pruebas médicas innecesarias (The $200 Billion Perils of Unnecessary Medical Tests) de la PBS.
-
- Aumentar el número de situaciones para las que se puede recetar o usar el medicamento es una estrategia conocida como “inventar enfermedades” (“disease mongering”).
Al examinar más de cerca un proceso concreto de aprobación de medicamentos, céntrate en aspectos clave que determinan el mercado del producto, comenzando con sus indicaciones. La indicación describe la condición aprobada para la que se puede usar un producto (medicamento, prueba, vacuna). Esto significa que las autoridades reguladoras han revisado las pruebas presentadas por el fabricante para el tratamiento, diagnóstico o prevención de una condición o enfermedad y han permitido a la empresa comercializar el producto para ese uso específico. Ampliar la indicación es una práctica común para incrementar el mercado de un producto, mientras la industria envía nuevos datos a los reguladores.
Sigue profundizando y analizando la definición de la enfermedad; cómo se describe y documenta el riesgo de desarrollarla; el diseño de los ensayos clínicos (resultados, criterios de exclusión/inclusión); los datos de eficacia y seguridad; y cómo se presentan los resultados del estudio. Cuando eres nuevo en el sector de la salud y de la atención médica, tienes que confiar mucho en la ayuda de científicos independientes para analizar la evidencia. Con el tiempo, serás cada vez más capaz de detectar signos de alerta y evaluar de forma independiente la evidencia. Tu revisión puede revelar a qué conclusiones erróneas se ha llegado sobre la relación riesgo-beneficio de un producto y dar una idea sobre cómo sucedió.
Profundizando aún más: bases de datos de ensayos clínicos
En 2005, el Comité Internacional de Editores de Revistas Médicas anunció que, para que sus estudios sean publicados, los patrocinadores que financian los ensayos clínicos tendrían que registrarlos antes de comenzar. En la actualidad, hay 24 registros (nacionales, regionales e internacionales, aquí está la lista). El portal de Búsqueda de Ensayos Clínicos de la OMS da acceso a una base de datos central, que contiene conjuntos de datos proporcionados por 17 registros, con enlaces a los originales.
Algunas empresas tienen sus propios registros, como GlaxoSmithKline y Eli Lilly. El primer registro virtual de este tipo fue ClinicalTrials.gov, que sigue siendo el más grande y utilizado. Los Institutos Nacionales de Salud de los Estados Unidos y la FDA trabajaron juntos para desarrollar el sitio, que es de acceso público desde febrero de 2000. Si estás considerando una investigación sobre una clase específica de fármacos o un medicamento, vale la pena comenzar en ClinicalTrials.gov.
Al buscar en bases de datos de ensayos clínicos debes revisar con atención la siguiente información:
- Diseño de estudio.
- Número de participantes.
- Criterios de inclusión/exclusión de participantes.
- Centros de investigación involucrados.
- Historia de los cambios.
- Si el ensayo sigue en curso.
- Si se publicaron los resultados.
- Resultados: primario, secundario, combinado, intermedio-sustituto. Es crucial entender el concepto de “resultado” si quieres investigar temas de salud y medicina. Según los Principios de la ciencia traslacional en medicina (Principles of Translational Science in Medicine), “los resultados clínicos son datos obtenidos en relación con una enfermedad en un estudio o en un ensayo clínico que reflejan el efecto de una intervención terapéutica/preventiva”. En algunos casos, los resultados/criterios de valoración intermedios-sustitutos se utilizan en lugar de resultados clínicamente importantes.
Puedes encontrar cambios en el diseño del estudio comparando los registros previos iniciales con los artículos publicados de los mismos estudios en las revistas científicas y/o presentados a agencias reguladoras. Incluso, como se ha comentado, los estudios no siempre terminan siendo publicados en revistas académicas. La falta de publicación y los cambios en el diseño de los estudios son signos de alerta importantes ya que podrían indicar la omisión de resultados problemáticos.
Durante el proceso de aprobación, las actas de las reuniones del comité asesor pueden ser reveladoras, ya que asesores y reguladores suelen ver problemas potenciales y hacen a la industria preguntas interesantes, a veces “inconvenientes”. Estas actas y los documentos te darán información sobre cuestiones y tensiones. Los sitios web de la FDA, la EMA y la OMS son un tesoro de información y te ofrecen posibles líneas de investigación.
Para conocer el papel de la OMS en la regulación de fármacos en el mundo, véase Regulación de drogas: historia, presente y futuro (Drug Regulation: History, Present and Future). La OMS también lleva la lista de medicamentos esenciales y la lista de pruebas diagnósticas esenciales, definida por la agencia como “documentos básicos de orientación que ayudan a los países a priorizar productos de salud críticos, que deben ser accesibles y tener precio razonable en los sistemas de salud”. Ambos documentos tienen un gran impacto en el mercado farmacéutico mundial.
Tercera sugerencia: obtén datos no publicados
No todos los documentos están en un registro público accesible, pero se pueden obtener de la FDA y EMA a través de una solicitud de libertad de información (FOI por sus siglas en inglés). Cuando haces esa solicitud puedes estar contribuyendo al bien común, ya que algunas solicitudes lograrán que algunos nuevos documentos acaben disponibles al público en el sitio web de la agencia.
Con iFOI, la herramienta desarrollada por el Comité de periodistas por la libertad de prensa, los usuarios registrados pueden crear, enviar, mantener y compartir solicitudes de información. En la Guía global de libertad de información de GIJN (Global Guide to Freedom of Information) encontrarás abundantes consejos y recursos de la ley FOI . Así mismo, considera usar la Ley de Promoción del Acceso a la Información de Sudáfrica (PAIA), que se aplica también a los organismos privados. Aunque la industria se resiste a cumplir con las solicitudes de divulgación completa con la excusa de que se pueden dañar los derechos de propiedad intelectual al exponer secretos industriales, si tu investigación se centra en una empresa con sede en Sudáfrica, vale la pena probar una solicitud de PAIA.
Si decides presentar una solicitud a la FDA, considera pedir acceso a la correspondencia por correo electrónico y documentos técnicos, así como a los datos estadísticos de los Planes de Análisis (DAP) de ensayos clínicos. En 2011, obtuvimos el documento DAP Merck presentado para obtener la aprobación de la vacuna contra el VPH Gardasil. El documento que publicamos en la revista BMJ Medicina Basada en la Evidencia permitió demostrar un ajuste metodológico significativo, introducido durante los ensayos en fase III. De forma que un análisis pre especificado fue reemplazado por un indicador de menor valor. Esta “conmutación de resultados” es una práctica controvertida y un problema potencial en los ensayos clínicos publicados, ya que puede distorsionar la evidencia.
Un ejemplo de las posibles consecuencias del cambio de resultados se discute en este informe de 2018 de la Academia Enago sobre el antidepresivo paroxetina, con enlaces a los estudios originales. El New York Times también abordó el tema en 2015, en este texto de Benedict Carey.
Para aprender más acerca de esta cuestión relativamente común en la práctica, echa un vistazo al proyecto COMPARE, desarrollado por un equipo de académicos, estudiantes de medicina y programadores en torno al CEBM de la Universidad de Oxford.
Los datos inéditos, no publicados de ensayos clínicos, pueden ser importantes al evaluar el perfil real de riesgo-beneficio de un fármaco. Pero obtener estos datos y realizar una evaluación puede ser difícil, incluso para científicos experimentados. Ve, por ejemplo, Estrategias para la obtención de datos inéditos del ensayo de fármacos: una entrevista cualitativa (Strategies for Obtaining Unpublished Drug Trial Data: A Qualitative Interview Study). Ten en cuenta, por ejemplo, que la FDA está legalmente autorizada a no confirmar ni negar la existencia de un estudio en respuesta a una solicitud. Hace poco, académicos y periodistas de investigación se han unido para localizar conjuntos de datos ausentes o incompletos.
Un ejemplo es la campaña de Tamiflu y otros antivirales del British Medical Journal, dirigida a presionar a las compañías farmacéuticas para que liberen los datos de estudios no publicados de dos medicamentos antigripales con los que se cuentan reservas estratégicas mundiales. Para tener una mayor comprensión de por qué la falta de transparencia importa y también saber de los grandes recursos para acceder a estudios no publicados puedes revisar estos recursos: Restauración de la iniciativa de ensayos invisibles y abandonados (Restoring Invisible & Abandoned Trials Initiative, AllTrials) y TranspariMED.